No products in the cart.
Hóa Chất Công Nghiệp, Tin tức
Điều chế H2SO4 Axit Sunfuric trong công nghiệp
Điều chế H2SO4 Axit Sunfuric trong công nghiệp. Tìm hiểu cách điều chế H2SO4 chi tiết trong công nghiệp, trong phòng thí nghiệm và lưu ý quan trọng khi điều chế bạn cần biết.
Điều chế H2SO4 như thế nào là câu hỏi được nhiều người quan tâm. Người ta tiến hành điều chế hợp chất này . Nhằm ứng dụng trong một số ngành công nghiệp, nông nghiệp, y tế, quân sự . Và giúp ích trong việc nghiên cứu tại phòng thí nghiệm. Tuy nhiên, đây là hợp chất Axit Sunfuric khá nguy hiểm . Cần phải điều chế đúng cách tránh ảnh hưởng đến sự an toàn. Cùng tìm hiểu cách điều chế chi tiết và những lưu ý quan trọng bạn cần biết khi điều chế hợp chất này trong bài viết dưới đây.

Điều chế H2SO4 trong công nghiệp
Axit Sunfuric là hợp chất hoá học được ứng dụng nhiều trong các ngành công nghiệp khác nhau. Như chất tẩy rửa, phân bón, phẩm màu, xử lý hóa chất. Để điều chế được hoá chất này trong công nghiệp bạn cần có kinh nghiệm thực tiễn. Tránh ảnh hưởng đến an toàn của chính bản thân và những người xung quanh.
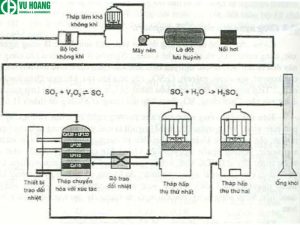
Cách điều chế H2SO4 trong công nghiệp là một quá trình gồm ba giai đoạn :
Giai đoạn 1:
Đốt cháy lưu huỳnh để tạo ra SO2. Lưu huỳnh được đốt cháy trong không khí ở nhiệt độ cao (khoảng 1000°C) . Để tạo ra khí SO2 theo phương trình:
S+O2→SO2
Giai đoạn 2:
Oxi hóa SO2 thành SO3. Khí SO2 được dẫn qua một bộ xúc tác chứa V2O5 ở nhiệt độ khoảng 450°C . Để tạo ra khí SO3 theo phương trình:
2SO2+O2→2SO3
Giai đoạn 3:
Hòa tan SO3 vào H2SO4 loãng để tạo ra H2SO4 đậm đặc. Khí SO3 được hòa tan vào H2SO4 loãng (98%) ở nhiệt độ thấp (khoảng 20°C) . Để tạo ra H2SO4 đậm đặc (98,5%) theo phương trình:
SO3+H2SO4→H2S2O7
H2S2O7 được gọi là Axit Sunfuric Pyrosulfuric hay Axit Sunfuric đôi. Nó có thể được phân hủy thành H2SO4 và SO3 bằng cách nung nóng.
H2S2O7→H2SO4+SO3
Xem thêm : >>> Axit Sunfuric liệu có độc? Lưu ý khi sử dụng axit H2SO4 hiện nay
Điều chế H2SO4 trong phòng thí nghiệm
Axit Sunfuric là một axit vô cơ mạnh, có công thức hóa học là H2SO4. Nó có tính oxi hóa mạnh, háo nước và có thể tác dụng với nhiều kim loại và phi kim. Để điều chế Axit Sunfuric, cần phải có các thiết bị và điều kiện phản ứng phức tạp. Không thể thực hiện được trong phòng thí nghiệm.
Cách điều chế Axit Sunfuric trong phòng thí nghiệm gồm có hai bước chính: đốt lưu huỳnh để tạo ra điôxít lưu huỳnh. Sau đó oxi hóa điôxít lưu huỳnh thành triôxít lưu huỳnh với sự có mặt của chất xúc tác oxit vanadi. Triôxít lưu huỳnh sau đó được hòa tan trong Axit Sunfuric đặc để tạo ra oleum. Rồi pha loãng với nước để được Axit Sunfuric mong muốn.
Quá trình tạo ra Axit Sunfuric trong tự nhiên
Axit Sunfuric được tạo thành trong tự nhiên bởi quá trình oxy hóa quặng pirit. Phân tử oxy oxy hóa quặng pirit sắt (FeS2) thành ion sắt (II) hay Fe2+:
2FeS2 + 7O2 + 2H2O → 2Fe2+ + 4SO42- + 4H+
Ion sắt (II) có thể bị oxy hóa lên ion sắt (III) hay Fe3+:
4Fe2+ + O2 + 4H+ → 4Fe3+ + 2H2O
Ion sắt (III) có thể tác dụng với ion sunfat (SO42-) để tạo ra kết tủa sắt (III) sunfat (Fe2(SO4)3):
2Fe3+ + 3SO42- → Fe2(SO4)3
Kết tủa sắt (III) sunfat có thể bị phân hủy bởi nước để tạo ra Axit Sunfuric và oxit sắt (III) hay Fe2O3:
Fe2(SO4)3 + 3H2O → 2Fe2O3 + 3H2SO4
Tham khảo thêm bài viết khác : >>> Axit H2SO4 là gì ? Tính chất và ứng dụng của axit sunfuric như thế nào ?
Lưu ý khi điều chế Axit Sunfuric H2SO4
Axit Sunfuric là một chất hóa học rất nguy hiểm đối với con người và môi trường sống. Nó có thể gây bỏng da, mắt, niêm mạc, hệ hô hấp, hệ tiêu hóa nếu tiếp xúc trực tiếp hoặc uống phải. Bỏng Axit Sunfuric có thể để lại sẹo không hồi phục được.
Ngoài ra, chất này có thể gây ho, sặc, khó thở, ngạt, viêm phổi nếu hít phải hơi Axit Sunfuric hoặc các khí SO2, SO3 do Axit Sunfuric phản ứng với các chất khác. Các khí này còn gây ô nhiễm không khí và ảnh hưởng đến sức khỏe cộng đồng.
Vì vậy, để điều chế Axit Sunfuric một cách an toàn nhất bạn cần đặc biệt lưu ý những vấn đề sau:
- Chú ý cần phải mặc đủ đồ bảo hộ, bao gồm kính bảo hộ, găng tay, quần áo, giày, khẩu trang. Vì đây là một chất hóa học rất nguy hiểm có thể ăn mòn và gây bỏng da, mắt, niêm mạc.
- Chú ý phải lưu trữ Axit Sunfuric ở nơi an toàn, khô ráo, thoáng mát, tránh ánh nắng trực tiếp. Không để gần nơi chứa bazơ hay chất khử.
- Phải chú ý sử dụng bồn nhựa, phuy nhựa, chai thủy tinh để đựng Axit Sunfuric, không dùng các thùng kim loại. Vì Axit Sunfuric có tính oxi hóa mạnh, có thể làm ăn mòn kim loại.
- Đậy nắp thật kín đáo, không đổ nó khỏi chai chứa, không pipette ra với miệng, không đun nóng Axit Sunfuric vì nó sẽ giải phóng ra các khí độc hại.
- Chú ý đổ từ từ Axit Sunfuric vào nước, tuyệt đối không được đổ nước vào Axit Sunfuric. Vì chất này rất háo nước.Có thể gây bỏng nặng cho những người đứng gần.
Kết luận :
Điều chế Axit Sunfuric không phải là điều dễ dàng. Vì vậy, cách tốt nhất là bạn nên tìm kiếm địa chỉ uy tín cung cấp loại hoá chất này. Hóa chất Vũ Hoàng hiện là một trong những cửa hàng bán hóa chất công nghiệp được đánh giá cao trên thị trường. Đơn vị cung cấp H2SO4 chất lượng, đảm bảo an toàn với mức giá phải chăng nhất. Đáp ứng được nhu cầu của khách hàng.
Bài viết trên là những chia sẻ về cách điều chế H2SO4 Axit Sunfuric. Và những lưu ý bạn cần chú ý khi điều chế để đảm bảo an toàn. Hy vọng những kiến thức này sẽ giúp bạn có thể tạo ra Axit Sunfuric đúng cách và ứng dụng vào trong sản xuất. Hãy liên hệ với hoá chất Vũ Hoàng qua HOTLINE 0945609898 hoặc Website : https://vuhoangco.com.vn để được tư vấn chi tiết về loại hoá chất này và cập nhật bảng giá ưu đãi nhất thị trường hiện nay.

