No products in the cart.
Hóa Chất Công Nghiệp, Tin tức
Cách điều chế NaOH kèm phương trình và hiện tượng
Cách điều chế NaOH kèm phương trình và hiện tượng . NaOH là hóa chất được ứng dụng rộng rãi trong ngành công nghiệp như xử lý nước, sản xuất giấy,… Tùy theo mục đích sử dụng và sản xuất mà NaOH có thể được điều chế theo nhiều phương pháp khác nhau. Bài viết dưới đây, Vũ Hoàng tổng hợp 5 phương pháp điều chế NaOH trong công nghiệp và phòng thí nghiệm. Theo dõi ngay!

Đôi nét về NaOH
Hóa chất NaOH là gì?
Natri hydroxit (NaOH), còn gọi là xút hoặc xút ăn da, là một bazơ mạnh. Có công thức hoá học đơn giản gồm một nguyên tử natri (Na), một nguyên tử oxi (O2) và một nguyên tử hydro (H). NaOH có dạng rắn, thường xuất hiện dưới dạng viên, hạt hoặc vảy trắng. Khi tan trong nước, NaOH tạo ra dung dịch kiềm mạnh, tỏa nhiều nhiệt.
Đặc tính nổi bật của NaOH là dễ hút ẩm, phản ứng nhanh với nước, axit và chất béo. Đây là hoá chất quan trọng trong nhiều lĩnh vực: sản xuất xà phòng, xử lý nước, chế biến thực phẩm,…
Nguồn gốc của NaOH
Có thể bạn đã biết, xút NaOH là hóa chất cực kỳ phổ biến với vô số ứng dụng trong sản xuất và đời sống. Thế nhưng, NaOH nguyên chất hoặc ở nồng độ cao lại không hề tồn tại trong tự nhiên. Có nghĩa là 100% sản lượng NaOH trên thế giới đều phải được sản xuất bằng phương pháp nhân tạo.
Nguyên nhân là do NaOH có tính hút ẩm mạnh, dễ hấp thụ hơi nước và CO₂ để tạo thành natri cacbonat. Đồng thời, nó có tính kiềm mạnh nên dễ dàng phản ứng với các chất trong tự nhiên. Tạo thành các hợp chất khác.
Trong khi đó, các nguyên tố giàu natri (Na) – thành phần tạo nên NaOH – lại rất phổ biến dưới dạng hợp chất bền. Như muối natri clorua (NaCl) trong nước biển hay các mỏ khoáng sản. Chính nguồn nguyên liệu dồi dào này đã mở ra điều kiện thuận lợi. Để điều chế NaOH phục vụ nhu cầu sử dụng ngày càng tăng.
Năm 2022, sản lượng Natri Hydroxit toàn cầu ước đạt 83 triệu tấn (dạng khô). Trong khi nhu cầu đạt khoảng 51 triệu tấn, tăng mạnh so với mức 45 triệu tấn của năm 1998. Sự tăng trưởng này cho thấy tầm quan trọng của việc liên tục điều chế NaOH để đáp ứng nhu cầu thị trường.
Cách điều chế NaOH Natri Hydroxit
NaOH là hóa chất có mặt trong nhiều quy trình sản xuất công nghiệp và cả trong các phòng thí nghiệm – nghiên cứu. Dưới đây 5 phương pháp sản xuất Natri Hydroxit phổ biến nhất hiện nay:
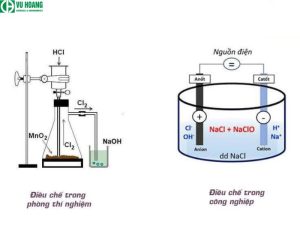
Cách điều chế NaOH trong công nghiệp bằng phương pháp điện phân dung dịch NaCl
Trong công nghiệp, NaOH được sản xuất bằng phương pháp điện phân dung dịch muối ăn (NaCl) có màng ngăn. Còn gọi là công nghệ Xút – Clo. Đây là cách điều chế hóa chất Natri Hydroxit quy mô lớn phổ biến nhất hiện nay . Vì có hiệu suất chuyển hóa cao và thân thiện với môi trường.
Quy trình điện phân dung dịch NaCl có màng ngăn để điều chế NaOH:
Bước 1: Chuẩn bị nguyên liệu là dung dịch muối ăn NaCl bão hoà
Muối ăn tinh khiết được hoà tan vào nước tạo thành dung dịch NaCl bão hoà. Sau đó được lọc để loại bỏ tạp chất như Ca²⁺, Mg²⁺.
Xem thêm : >>> Xút vảy (NaOH) 99% hoá chất điều chỉnh pH – Giải pháp hiệu quả cho ngành công nghiệp
Bước 2: Đưa dung dịch vào bình điện phân có màng ngăn ion
Ngăn dương và ngăn âm, được ngăn cách bởi màng trao đổi ion, cho phép ion Na⁺ đi qua nhưng chặn Cl⁻ và OH⁻.
Bước 3: Tiến hành điện phân
- Tại cực dương:
2Cl− → Cl2↑ + 2e−
→ khí Clo được sinh ra
- Tại cực âm:
2H2O + 2e− → 2OH− + H2↑
→ sinh khí hydro và ion H-
Bước 4: Di chuyển ion và tạo thành NaOH
Ion Na+ từ dung dịch muối di chuyển qua màng ngăn đến cực âm . Và kết hợp với OH- tạo thành dung dịch NaOH loãng.
Bước 5: Thu hồi sản phẩm
- Khí Cl2 được dẫn ra ngoài để sử dụng trong công nghiệp hoá chất (sản xuất PVC, HCl,…)
- Khí H2 được thu hồi dùng làm nhiên liệu hoặc nguyên liệu hoá học
- Dung dịch NaOH loãng được cô đặc bằng bay hơi để thu được NaOH 30-50%. Có thể tiếp tục cô đặc để tạo thành dạng rắn.
Phương trình điều chế NaOH trong công nghiệp như sau:
2NaCl + 2H2O → 2NaOH + H2 + Cl2
Điện phân dung dịch có màng ngăn là cách tạo ra NaOH được sử dụng phổ biến trên toàn cầu. Phương pháp này có một số ưu và nhược điểm như sau:
Ưu điểm:
- Quy trình có hiệu suất chuyển hóa cao, phù hợp để sản xuất NaOH với khối lượng lớn.
- NaOH thu được có độ tinh khiết cao, đáp ứng yêu cầu của nhiều ngành công nghiệp.
- Đây là phương pháp kinh tế và hiệu quả nhất cho quy mô công nghiệp lớn.
- Khí Clo và Hydro là các sản phẩm phụ quan trọng, có thể được thu hồi và bán. Hoặc sử dụng trong các ngành công nghiệp khác, tăng thêm lợi ích kinh tế.
Nhược điểm:
- Quá trình điện phân tiêu thụ một lượng lớn năng lượng điện.
- Đòi hỏi công nghệ và thiết bị chuyên dụng (màng ngăn) để đảm bảo an toàn và hiệu quả.
Tham khảo thêm : >>> Bột Xút (NaOH): Đặc Tính, Ứng Dụng, Cách Sử Dụng An Toàn
Cách điều chế NaOH trong phòng thí nghiệm
Trong phòng thí nghiệm, NaOH là một hóa chất rất quan trọng. Nó được dùng để chuẩn độ axit, điều chỉnh độ pH. Làm khô không khí và tham gia vào nhiều phản ứng hóa học. Để tạo ra chất Natri Hydroxit trong nghiên cứu và giảng dạy. Người ta thường dùng một trong 4 phương pháp dưới đây:
Cho kim loại Natri tác dụng với nước
Đây là một trong những cách đơn giản nhưng cực kỳ mạnh mẽ để điều chế NaOH từ kim loại kiềm.
- Nguyên liệu để sản xuất NaOH: Kim loại Natri (Na) và Nước (H2O).
- Hiện tượng: Kim loại Natri phản ứng mãnh liệt với nước, tạo ra khí không màu (H2) và dung dịch NaOH. Phản ứng tỏa nhiều nhiệt, có thể làm nóng chảy Natri. Thậm chí gây cháy hoặc nổ khí H2.
- Phương trình phản ứng:
2Na + 2H2O → 2NaOH + H2
- Ưu điểm: Đơn giản, dễ thực hiện để minh hoạ tính chất hoá học của kim loại.
- Nhược điểm: Cực kỳ nguy hiểm, phản ứng rất mãnh liệt có thể gây cháy hoặc nổ. Không phù hợp cho sản xuất quy mô lớn.
Cho oxit Natri tác dụng với nước
Phương pháp này điều chế NaOH bằng cách cho oxit bazơ tan của Natri phản ứng với nước.
- Nguyên liệu để sản xuất NaOH: Natri Oxit (Na2O) và nước (H2O)
- Hiện tượng: Natri Oxit là một bazơ tan trong nước, phản ứng tạo ra dung dịch NaOH. Phản ứng toả nhiệt.
- Phương trình phản ứng :
Na2O + H2O → 2NaOH
- Ưu điểm: Đơn giản, dễ thực hiện, ít nguy hiểm hơn so với cho Natri tác dụng trực tiếp với nước.
- Nhược điểm: Natri Oxit (Na2O) là hoá chất đắt tiền và khó bảo quản (dễ phản ứng với không khí ẩm). Không phù hợp cho sản xuất công nghiệp.
Cho soda Na2CO3 tác dụng với vôi tôi
Đây là phương pháp cũ, từng được sử dụng để điều chế NaOH trước khi phương pháp điện phân trở nên phổ biến.
- Nguyên liệu để sản xuất NaOH: Natri Cacbonat (Na2CO3 – Soda) và canxi hidroxit (Ca(OH)2 – Vôi tôi).
- Hiện tượng: Hai chất này phản ứng với nhau trong dung dịch, tạo ra NaOH tan và Canxi Cacbonat (CaCO3) kết tủa trắng.
- Phương trình hoá học:
Na2CO3 + Ca(OH)2 → CaCO3 + 2NaOH
- Ưu điểm: Sử dụng các nguyên liệu tương đối rẻ và dễ kiếm.
- Nhược điểm: NaOH thu được cần được lọc tách khỏi kết tủa CaCO3. Dung dịch NaOH thường loãng và có thể chứa tạp chất (do Ca(OH)2 tan ít). Đây là phương pháp cũ, ít được dùng trong công nghiệp hiện đại.
Cho Natri Hiđrua (NaH) tác dụng với nước
Phương pháp này điều chế NaOH từ một hợp chất hidrua kim loại. Thường dùng để minh hoạ tính chất hoá học của NaH.
- Nguyên liệu để sản xuất NaOH: Natri Hiđrua (NaH) và nước (H2O).
- Hiện tượng: Natri Hiđrua là một chất khử mạnh, phản ứng mãnh liệt với nước tạo ra NaOH và khí Hydro (H2). Phản ứng toả nhiệt.
- Phương trình phản ứng:
NaH + H2O → NaOH + H2
- Ưu điểm: Đơn giản để minh họa phản ứng.
- Nhược điểm: Natri Hiđrua (NaH) là hoá chất rất đắt tiền, cực kỳ dễ cháy nổ khi tiếp xúc với nước . Và không phù hợp cho sản xuất quy mô lớn.
NaOH công nghiệp mua ở đâu chất lượng?
Nếu bạn đang loay hoay không biết nên mua xút NaOH ở đâu. Thì Vũ Hoàng chính là địa điểm đáng tin cậy dành cho bạn. Vũ Hoàng chuyên cung cấp NaOH tinh khiết 99% và có nguồn gốc rõ ràng. Để biết chi tiết hơn về sản phẩm, hãy liên hệ ngay với Vũ Hoàng qua số HOTLINE 0945609898 . Vũ Hoàng luôn sẵn lòng cung cấp thông tin và hỗ trợ bạn tìm được sản phẩm phù hợp với mức giá tốt nhất.

